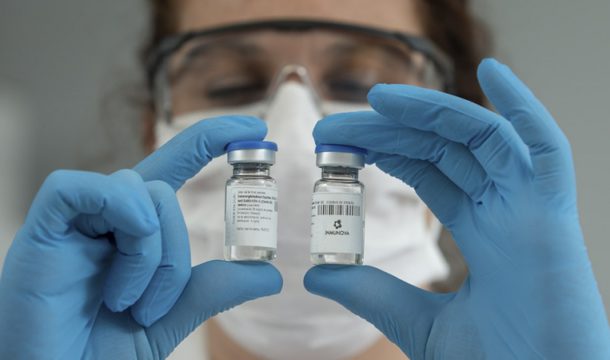
ANMAT aprobó el suero equino hiperinmune para tratar casos moderados y severos de Covid-19
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat) aprobó, bajo registro de condiciones especiales, para pacientes moderados y severos, el suero equino hiperinmune desarrollado por el laboratorio Inmunova. Además, las conclusiones del estudio fueron enviadas a una revista científica internacional para su constatación.
“Cumpliendo con los más altos estándares internacionales de buenas prácticas clínicas, el estudio evaluó la seguridad y eficacia de este medicamento basado en anticuerpos policlonales”, publicó la firma Inmunova, y señaló que el estudio “evalúa su seguridad y eficacia en pacientes voluntarios con enfermedad moderada a severa por SARS-Cov-2 dentro de los 10 días de síntomas y que requiere hospitalización”.
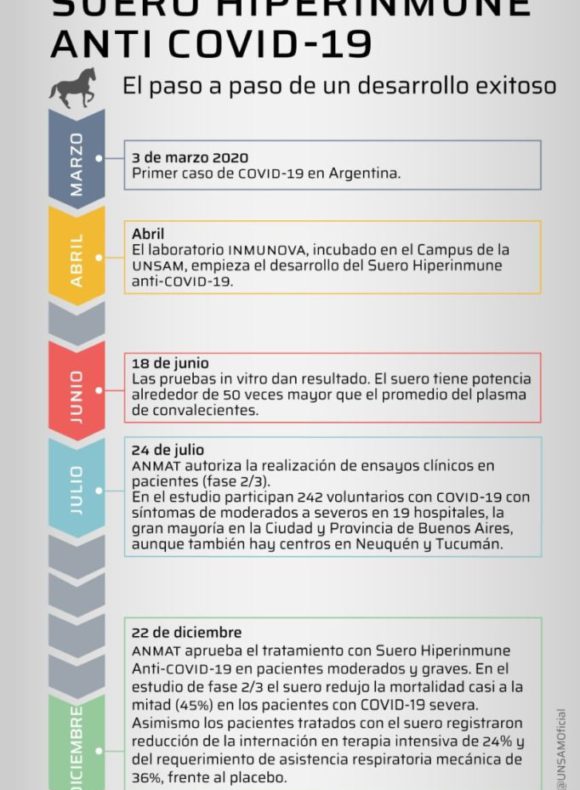
La aprobación de este medicamento innovador basado en anticuerpos policlonales se fundamentó en los resultados positivos del estudio clínico de Fase 2/3 de INM005, los cuales mostraron que la aplicación de esta terapia, que demostró ser segura, redujo la mortalidad casi a la mitad (45%) en los pacientes con COVID-19 severa.
Asimismo, los pacientes tratados con INM005 registraron reducción de la internación en terapia intensiva de 24% y del requerimiento de asistencia respiratoria mecánica de 36%, frente al placebo. Además, mostraron beneficio clínico considerable a lo largo de los 28 días de seguimiento del tratamiento y mejora significativa de dos puntos en la escala ordinal de evaluación clínica de ocho puntos de la OMS a los 7, 14 y 21 días.
Asimismo, se indicó que “en el estudio se realizaron análisis interinos de seguridad a cargo de un comité independiente de médicos especialistas, que fueron positivos”.
La investigación incluyó la participación voluntaria de 242 pacientes adultos con enfermedad moderada a severa causada por el SARS-CoV-2 confirmada por PCR.
Según afirmó Linus Spatz, director de Inmunova, “el estudio clínico nos permitió determinar mediante el método científico que nuestro tratamiento anti-SARS-CoV-2 es seguro y eficaz con un beneficio clínico considerable, en especial en la población de pacientes severos, disminuyendo la progresión e impacto de la enfermedad”. Y agregó: “Nos satisface poder contribuir con una opción terapéutica para mitigar los efectos de la COVID-19 y estamos trabajando en la producción del medicamento para asegurar el suministro que sea necesario”.
Inmunización pasiva
La inmunización pasiva, principio de este desarrollo, consiste en administrar anticuerpos a los pacientes contra el agente infeccioso, produciendo su bloqueo y evitando que se propague. Así actúa el suero, que es similar a los que se usan para tratar el envenenamiento por picadura de serpientes y alacranes, intoxicaciones por toxina tetánica, exposición al virus de la rabia e infecciones como la influenza aviar.
Fernando Goldbaum, investigador del CONICET en el Centro de Rediseño e Ingeniería en Proteínas (CRIP, UNSAM) y socio-fundador y director científico de Inmunova, explicó a mediados de año, cuando recién comenzaban este desarrollo científico: “A diferencia de las vacunas (inmunización activa) que permiten que una persona genere preventivamente sus propios anticuerpos contra determinados patógenos, el suero terapéutico introduce desde afuera anticuerpos que pueden actuar rápidamente en un paciente que ya está infectado. Cuando nos cortamos con un alambre, por ejemplo, lo primero que hacen en darnos un suero antitetánico y luego la vacuna”.
El suero desarrollado se basa en anticuerpos policlonales equinos, que se obtienen mediante la inyección de una proteína recombinante del SARS-CoV-2 en los caballos, inocua para ellos, de modo que tienen la capacidad de generar gran cantidad de anticuerpos capaces de neutralizar el virus.
“La ventaja de este suero respecto del uso de plasma convalecientes- estrategia que también apoyamos y que ha mostrado hasta ahora ser la más segura y eficaz- es que en caso de que funcione se puede escalar su producción para tratar también pacientes en etapas tempranas de la enfermedad. Sería posible producirlo para toda la población que lo necesite”, explicó Goldbaum.
Los ensayos se llevaron a cabo en distintos centros sanitarios del país. El suero hiperinmune fue probado en CABA en el Sanatorio Güemes; el Hospital General de Agudos “Dr. Ignacio Pirovano”; el Hospital Italiano de Buenos Aires; el Centro Gallego de Buenos Aires; la Clínica Adventista Belgrano; el Sanatorio Sagrado Corazón; el Hospital de Infecciosas “Francisco Muñiz”; la Clínica Zabala; el Sanatorio Agote; la Fundación Favaloro; y el Hospital Español. En la provincia de Buenos Aires, en el Instituto Médico Platense; en el Hospital Italiano (La Plata); en el Hospital Cuenca Alta – SAMIC (Cañuelas); en el Hospital “Profesor Dr. Bernardo Houssay” (Vicente López); en el Hospital El Cruce (Florencio Varela); en el Hospital Municipal “Emilio Zerboni” (San Antonio de Areco); y en el Hospital Municipal “Dr. Diego Thompson” (San Martín). En Neuquén, fue probado en Hospital Provincial “Dr. Eduardo Castro Rendón”, y en Tucumán, en el Hospital Centro de Salud Zenón Santillán.
El desarrollo del suero equino hiperinmune se logró gracias al trabajo de articulación pública-privada encabezado por el laboratorio Inmunova y el Instituto Biológico Argentino (BIOL), la Administración Nacional de Laboratorios e Institutos de Salud “Dr. Carlos G. Malbrán” (ANLIS), con la colaboración del CONICET, la Fundación Instituto Leloir (FIL), Mabxience y la Universidad Nacional de San Martín (UNSAM). (DIB) AR
Deja un comentario




















.png)












